APAP在肝脏的代谢是通过转化成一种毒性代谢物N-乙酰苯醌亚胺(NAPQI)进行的。此毒性化合物可以干扰线粒体电子传递链复合物I/II,导致细胞内O2•−含量升高。O2•−可与内源性一氧化氮(NO)反应生成ONOO−。由于这些ROS和RNS由不同通路产生,并具有不同的生物学功能,因此高灵敏度、高选择性地同时检测它们有助于进一步了解药物诱导的肝损伤的发生发展机制,从而采取有效预防和治疗。
荧光成像法具有非侵入式、高灵敏度、操作简便等优势,广泛应用于细胞活体内活性分子的成像检测。NIR荧光成像具有自发荧光低且减少组织中的光散射等优点。迄今为止,已经报道了许多NIR荧光探针用于检测O2•−,但是用于评估药物诱导肝损伤过程中O2•−含量变化的理想工具尚未报道。相比于单光子(OP)荧光成像,TP荧光成像具有组织穿透深度更深、时空分辨率更高等优势。然而,应用于研究ONOO−在药物诱导的肝损伤中作用的TP激发探针仍然很少。
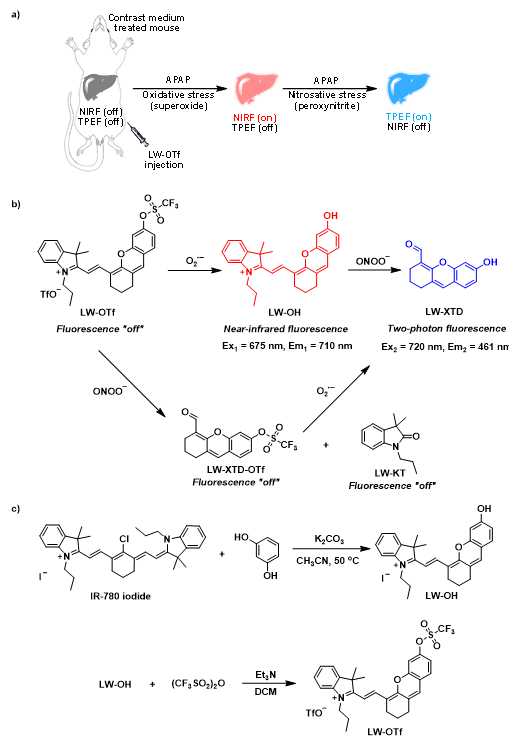
图 1 荧光探针LW−OTf的设计与合成。
为了解决这一难题,山东师范大学化学化工与材料科学学院李平教授、唐波教授课题组与英国巴斯大学化学系Tony D. James教授课题组经过不懈努力,成功构建了首个兼具近红外发射和双光子激发性质的反应型小分子荧光探针。LW−OTf的设计策略和合成路线如图1所示。O2•−触发LW−OTf中三氟甲磺酸酯基团脱保护,通过产生NIR荧光团LW−OH,导致NIR红色荧光信号增加。随后与ONOO−反应导致LW−OH的C=C氧化裂解,生成具有TP性质的氧杂蒽衍生物LW−XTD。
在模拟生理条件下,作者首先评估了LW−OTf的单、双光子性能。结果表明,探针具有高选择性、高灵敏度和高生物相容性,非常适用于O2•−和ONOO−的生物成像研究。
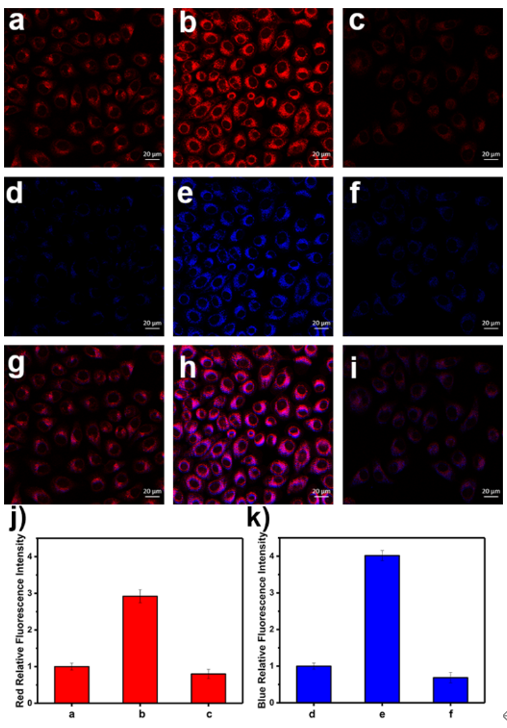
图 2 LW−OTf用于动态监测APAP诱导的肝损伤过程中O2•−和ONOO−含量变化。
作者使用双光子荧光显微镜评估了LW−OTf在APAP诱导的肝损伤中的性能。成像结果显示,与正常细胞相比,APAP诱导的肝细胞中表现出强烈的红色荧光和蓝色荧光,说明LW−OTf能够灵敏地检测出APAP诱导的肝损伤模型中肝细胞内源性O2•−和ONOO−的爆发(图2)。同时,LW−OTf成功监测到BHA对APAP诱导肝细胞毒性的化学保护作用。
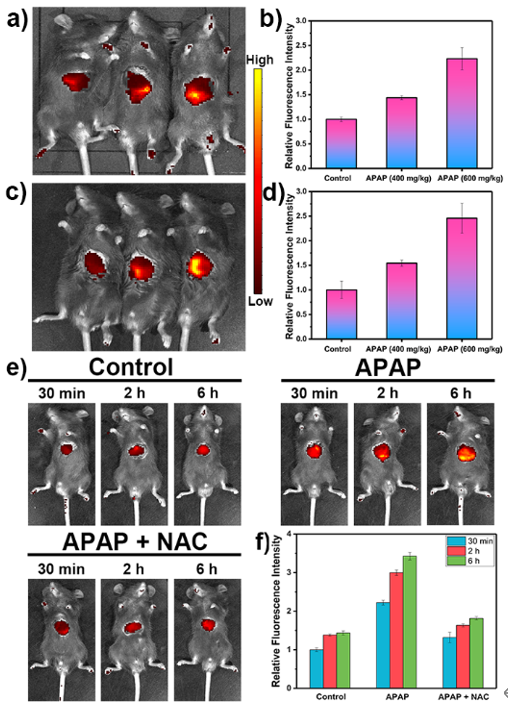
图 3 LW−OTf用于动态监测APAP诱导的小鼠肝损伤过程中O2•−变化。
在上述活细胞研究结果的鼓舞下,作者将LW−OTf用于活体成像,以追踪APAP诱导的小鼠肝损伤过程中O2•−和ONOO−的含量变化。使用200 mg/kg剂量(对照组)和400 mg/kg和600 mg/kg剂量(实验组)的APAP处理C57小鼠。如图3a,在给予高剂量的APAP后,小鼠裸露的肝脏表现出浓度依赖的荧光增强(~710 nm)。作者进一步验证了LW−OTf具有穿透深度深的优势,可适用于小鼠深层组织成像。结果显示脱毛小鼠的实验组均表现出明显的荧光增强(图3c)。和接下来,作者探究了APAP不同的给药时间对小鼠肝损伤的作用结果(图3e)。结果表明最高剂量组(APAP 600 mg/kg)随着时间的推移,NIR荧光明显增强,表明药物诱导的肝损伤过程中ROS持续产生。为了证实这一点,作者将保肝药物N-乙酰半胱氨酸(NAC)注射到肝损伤小鼠(APAP 600 mg/kg)体内,结果表明,NAC使荧光信号明显衰减,恢复到与对照组小鼠相当的水平(图3f)。
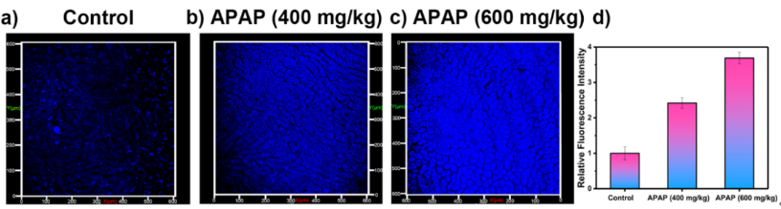
图 4 LW−OTf用于动态监测APAP诱导的小鼠肝损伤过程中ONOO−变化。
作者利用NIR荧光成像成功追踪到APAP诱导的小鼠肝损伤过程升高的O2•−后,随后将注意力转移到使用TP成像实时监测小鼠肝损伤过程中ONOO−的水平变化。在720 nm波长激发下,在小鼠肝损伤组织中观察到3.68倍的荧光增强(图4)。这些结果证明了LW-OTf兼具NIR成像高灵敏度和TP成像的高组织穿透性等优点,能够实现高灵敏度成像检测APAP诱导的肝损伤中O2•−和ONOO−。
综上,作者开发了NIR、TP双模态荧光探针,首次成功实现了在活细胞和小鼠中对与药物诱导肝损伤相关的RNS和ROS进行实时、原位成像。LW−OTf的分子设计策略可以推广到药物诱导肝损伤中其他生物标志物(如磷酸酯酶和ONOO−)的双检测。这一工作为揭示药物诱导肝损伤分子机制等研究提供了新的工具,并有助于开发治疗药物诱导肝损伤的新方法。
该研究工作得到了国家自然科学基金、国家重大新药创制项、国家留学基金委、山东省重点研发计划、英国皇家学会和英国巴斯大学的大力资助。英国巴斯大学博士研究生吴庐陵和山东师范大学博士研究生刘继红为该论文的共同第一作者。山东师范大学为第一单位。李平教授、唐波教授和Tony D. James教授为共同通讯作者。
原文链接:https://doi.org/10.1039/D0SC05937D
原文引用:DOI: 10.1039/d0sc05937d
 客服热线:
客服热线: